钢铁工业是国家工业的基础。请回答钢铁冶炼、腐蚀、防护过程中的有关问题。
(1)工业用热还原法炼铁,写出由CO还原赤铁矿(主要成分为Fe2O3)的化学方程式:
。
(2)下列可防止铁棒被腐蚀装置是 。
(3)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如下:

请回答:A电极对应的金属是______(写元素名称),B电极的电极反应式是 。
镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因
。
(1)3CO+Fe2O3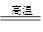 2FW+3CO2 (2)BD (3)铜 Cu2++2e-=Cu 镀铜铁破损后,金属铁为负极,镀锌铁破损后,金属铁是正极,负极金属易被腐蚀
2FW+3CO2 (2)BD (3)铜 Cu2++2e-=Cu 镀铜铁破损后,金属铁为负极,镀锌铁破损后,金属铁是正极,负极金属易被腐蚀
题目分析:(1)CO具有还原性,则还原赤铁矿(主要成分为Fe2O3)的化学方程式是3CO+Fe2O3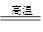 2FW+3CO2。
2FW+3CO2。
(2)在B原电池装置中,正极金属铁被保护,在电解池装置D中,阴极铁金属被保护,A装置中,金属铁做原电池的负极,更易被腐蚀,在C装置中,金属铁和水以及少量的氧气接触,也会被腐蚀,故答案为BD。
(3)在铁件的表面镀铜的电镀池中,作阳极的是镀层金属铜,所以根据装置图可知,A电极和电源的正极相连,做阳极,则A是铜。B电极和电源的负极相连,做阴极,则做阴极的是待镀金属铁,该极上金属阳离子铜离子发生得电子的还原反应,即Cu2++2e-=Cu。镀铜铁破损后,金属铁为负极,镀锌铁破损后,金属铁是正极,在原电池中,负极金属更易被腐蚀,所以镀铜铁比镀锌铁更容易被腐蚀。
点评:本题是一道有关金属的腐蚀和防护知识的考查题,侧重对学生基础知识的巩固和训练。旨在培养学生灵活运用基础知识解决实际问题的能力。本题注意知识的积累和教材知识的灵活应用是解题的关键,难度不大。
