I.铝的阳极氧化能使铝的表面生成一层特别致密的氧化膜,该氧化膜不溶于稀硫酸,模拟该生产过程如下:
(1)把铝片浸入热的16%NaOH溶液中约半分钟左右洗去油污,除去表面的氧化膜,取出用水冲洗。写出除去氧化膜有关反应的离子方程式____________
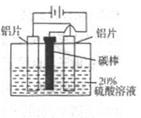
(2)如图,组装好仪器,通电约25min。在阳极生成氧化铝,阴极产生气体。则该过程中阳极发生反应的电极式为______;该溶液pH的变化______(填:“增大”或“减小”或“不变”)
II现代社会对电池的需求越来越大,尤其足可充电的二次电池。
髙铁电池是一种新型可充电电池,总反应为:3Zn(OH)2+2Fe(OH)3+4KOH 3Zn+2K2FeO4+8H2O,该电池放电时正极材料的化学式是 其电极反应式是______,若电路中通过1.204×1023个电子时,负极质量变化为______g充电时,该电池的正极接直流电源的______(填“正极”或“负极”)。
3Zn+2K2FeO4+8H2O,该电池放电时正极材料的化学式是 其电极反应式是______,若电路中通过1.204×1023个电子时,负极质量变化为______g充电时,该电池的正极接直流电源的______(填“正极”或“负极”)。
(16分)
Ⅰ.(1)Al2O3+2OH-+3H2O=2[Al(OH)4]-(2分)
(2)2Al+3H2O-6e-=Al2O3+6H+(2分);减小(2分)
Ⅱ.K2FeO4(1分)FeO42-+4H2O+3e-=Fe(OH)3+5OH-(2分);6.5(2分);正极(1分)
题目分析:
Ⅰ.(1)结合题目知氧化铝与NaOH反应:Al2O3+2OH-+3H2O=2[Al(OH)4]-
(2)铝在阳极放电在阳极生成氧化铝,2Al+3H2O-6e-=Al2O3+6H+;总反应2Al+6H2O=Al2O3+6H2↑,只是消耗水,所以酸的浓度增大,pH减小。
Ⅱ.总反应为:3Zn(OH)2+2Fe(OH)3+4KOH 3Zn+2K2FeO4+8H2O,正极材料的化学式是K2FeO4;负极反应:Zn+2OH--2e-=Zn(OH)2,可知正极电极反应式是FeO42-+4H2O+3e-=Fe(OH)3+5OH-;电路中通过1.204×1023个电子时,负极反应Zn0.1mol;充电时,该电池的正极应该发生氧化反应,做阳极,接在电源的正极。
3Zn+2K2FeO4+8H2O,正极材料的化学式是K2FeO4;负极反应:Zn+2OH--2e-=Zn(OH)2,可知正极电极反应式是FeO42-+4H2O+3e-=Fe(OH)3+5OH-;电路中通过1.204×1023个电子时,负极反应Zn0.1mol;充电时,该电池的正极应该发生氧化反应,做阳极,接在电源的正极。
