问题
选择题
如图甲、乙是电化学实验装置。有关电极反应或计算错误的是:
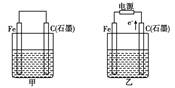
A.若甲烧杯中盛有NaCl溶液,则石墨棒上的电极反应式为O2+2H2O+4e-= 4OH-
B.若乙烧杯中盛有则乙中的总反应为
C.若甲烧杯中盛有CuSO4溶液,则甲中铁棒上的电极反应式为Fe-2e-=Fe2+
D.若起始时乙中盛有200 mL pH=5的CuSO4溶液,一段时间后溶液的pH变为1,若要使溶液恢复到电解前的状态,可向溶液中加入0.6 g CuO
答案
答案:D
题目分析:A、若甲烧杯中溶液为氯化钠溶液,类似于钢铁的吸氧腐蚀,石墨棒是正极电极反应式为O2+2H2O+4e-= 4OH-,正确;B、若乙烧杯盛NaCl溶液,据电子的流向可知石墨是阳极,铁做阴极则乙中的总反应为2Cl-+2H2O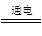 2OH-+H2↑+Cl2↑,正确;C、此时铁做负极,正确;D、一段时间后溶液的PH为1,此时溶液中H+的物质的量浓度为0.1mol/L,其物质的量为0.2mol,忽略水电离出的氢离子,电解总反应式为2Cu2++2H2O
2OH-+H2↑+Cl2↑,正确;C、此时铁做负极,正确;D、一段时间后溶液的PH为1,此时溶液中H+的物质的量浓度为0.1mol/L,其物质的量为0.2mol,忽略水电离出的氢离子,电解总反应式为2Cu2++2H2O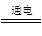 4H++O2↑+2Cu,要使溶液恢复原状态,可加入CuO,一段时间后溶液的pH变为1,则c(H+)=0.1mol/L-10-5mol/L=0.1mol/L,n(H+)=0.2L×0.1mol/L=0.02mol,则由电解反应可知析出的Cu的物质的量为0.01mol,由Cu原子守恒可知,m(CuO)=0.01mol×80g/mol=0.8g,错误。
4H++O2↑+2Cu,要使溶液恢复原状态,可加入CuO,一段时间后溶液的pH变为1,则c(H+)=0.1mol/L-10-5mol/L=0.1mol/L,n(H+)=0.2L×0.1mol/L=0.02mol,则由电解反应可知析出的Cu的物质的量为0.01mol,由Cu原子守恒可知,m(CuO)=0.01mol×80g/mol=0.8g,错误。
