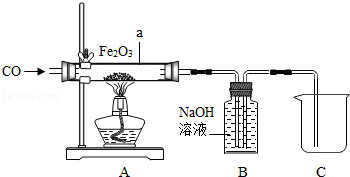
化学兴趣小组的同学设计了用一氧化碳气体还原氧气铁的实验装置,如图所示,回答下列问题:
(1)为了避免玻璃管a在加热时可能发生爆炸,加热前应 .
(2)a管中Fe2O3发生反应的化学方程式为 .
(3)B装置除了吸收CO2气体外,还 .写出B装置中NaOH发生反应的化学方程式 .
(4)若a管中氧化铁全部还原成铁,冷却后称量铁的质量比反应前氧化铁的质量减少了2.4g,则加入a管中的氧化铁的质量是 g.
(1)先通一氧化碳排尽玻璃管内空气;
(2)3CO+Fe2O3 2Fe+3CO2;
2Fe+3CO2;
(3)可收集纯净的一氧化碳,防止一氧化碳逸出污染空气;CO2+2NaOH═Na2CO3+H2O;
(4)8.
题目分析:(1)一氧化碳具有可燃性,与空气混合,加热可能会发生爆炸,所以在加热前要先通一氧化碳排尽玻璃管内空气防止一氧化碳不纯发生爆炸;
(2)在高温条件下,一氧化碳与氧化铁反应生成铁和二氧化碳,反应的化学方程式为3CO+Fe2O3 2Fe+3CO2;
2Fe+3CO2;
(3)装置C内盛有氢氧化钠溶液可以除去尾气中的二氧化碳,同时一氧化碳气体排出装置内的溶液而被收集,防止造成空气污染;二氧化碳与氢氧化钠溶液反应生成碳酸钠和水,方程式是:CO2+2NaOH═Na2CO3+H2O;
(4)氧化铁Fe2O3中Fe与O元素的质量比=(56×2):(16×3)=7:3,因此,氧化铁中氧元素质量为2.4g时,铁元素的质量=2.4g×=5.6g,则氧化铁的质量为:2.4g+5.6g=8g;
点评:运用对一氧化碳还原氧化铁反应操作的理解,推断各装置的作用,并能进行简单的分析和计算,是解答类似问题的一般方法.
