问题
选择题
依据甲、乙、丙三图回答下列问题:
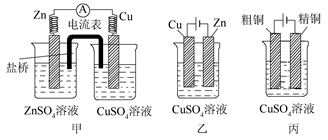
(1)甲装置为__________,乙装置为__________,丙装置为__________。
(2)甲、乙装置中,锌极上分别发生__________反应、__________反应。
(3)乙装置中,Cu2+浓度__________。
答案
(1)原电池 电镀池 电解精炼铜(乙丙装置回答电解池同样给分)
(2)氧化 还原 (3)不变 (每空1分,共6分)
题目分析:(1)根据装置图可知,甲装置中含有盐桥,且含有活泼性不同的金属以及电解质溶液,所以甲装置是原电池;乙装置中含有外接电源,锌与电源的负极相连,做阴极。铜与电源的正极相连,做阳极,铜失去电子。电解质溶液是硫酸铜,所以乙装置是电镀池;丙装置中含有外接电源,粗铜与电源的正极相连,做阳极。纯铜与电源的负极相连,硫酸铜是电解质溶液,所以丙装置是电解精炼铜。
(2)锌的金属性强于铜,所以甲装置中锌是负极,发生氧化反应;乙装置中锌与电源的负极相连,做阴极,发生还原反应。
(3)乙装置中阳极铜失去电子,阴极铜离子得到电子,所以溶液中铜离子的浓度不变。
