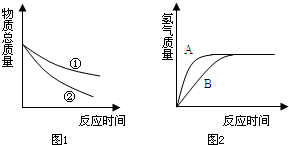
小红和小明进行盐酸与锌反应制取氢气的实验研究.小红用较稀的盐酸,小明用较浓的盐酸.他们分别取等质量的锌粒与等质量盐酸在烧杯中反应,(假设盐酸均足量)并将烧杯中物质总质量随反应时间的变化情况绘制成图1.
试回答下列问题:
(1)烧杯中物质总质量减少的原因是______;
(2)表示小红实验结果的是图中的曲线______(填①或②);
(3)请说明图中的曲线②与曲线①不同的原因______.
(4)图2是小李同学绘制的小红与小明各自实验中产生纯氢气随时间变化的情况,请指出表示小明实验的曲线是______(填“A”或“B”)
(1)锌能与盐酸反应生成氢气逸出、盐酸具有挥发性、反应放热导致水分蒸发,从而使烧杯内物质的总质量减小.故答案为:反应放出氢气、氯化氢气体逸出、反应放热导致水分蒸发;
(2)小红用的是稀盐酸,反应较慢,相同时间内生成氢气较少;稀盐酸挥发性较小.因此相同时间内烧杯内物质的总质量比用浓盐酸时剩余的多.表现在图象上就是锌与稀盐酸反应的曲线比与浓盐酸的高.故答案为:①;
(3)图中的曲线②与曲线①不同的原因是:曲线②浓盐酸,浓度较大,逸出的氯化氢气体多;并且与锌反应速度较快,曲线下降快,故其质量减小较快;故答案为:a.曲线②盐酸浓度较大,反应速率较快,所以曲线下降较快b.曲线②盐酸浓度较大,逸出的氯化氢气体多,所以最后位置较低;
(4)因为小明用的是浓盐酸,反应速率快,比小红的实验用的时间少.故填:A
