化学实验小组在实验室制备氢气时,发现没有锌粒或铁屑,仅有一些碎铝片.根据有关资料提示,他们将铝片放入烧碱溶液中,除去表面的氧化膜(Al2O3),洗净后用于制取氢气.
回答下列问题:
(1)已知氧化铝与烧碱溶液反应时,会生成偏铝酸钠(NaAlO2)和水,写出该反应的化学方程式______.
(2)图中是实验小组组装的制取氢气的发生装置,检验该装置气密性的方法是______.
(3)用金属铝和稀盐酸反应制取氢气的化学方程式是______.
(4)收集氢气的常用方法是______.
(5)在相同温度下,若用锌片和铝片分别与相同浓度的盐酸反应制取氢气,反应速率:锌______铝(填“>”“=”“<”),理由是______.
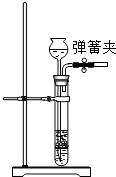
氧化铝与烧碱反应的化学方程式为Al2O3+2NaOH=2NaAlO2+H2O;检查装置的气密性关闭弹簧夹,从长颈漏斗中慢慢注水至淹没长颈漏斗下端管口,形成密封的空间,向长颈漏斗中注入少量水,至漏斗颈部形成水柱,静置,观察水柱是否下降,若不下降则气密性良好;氢气的密度小于空气密度,难溶于水,因此既可以用向下排空气法收集又可以用排水法收集;铝的活动性比镁的活动性强,所以用锌片和铝片分别与相同浓度的盐酸反应制取氢气时,铝的反应速率比锌的反应速率大.
故答案为:(1)Al2O3+2NaOH=2NaAlO2+H2O
(2)关闭弹簧夹,从长颈漏斗中慢慢注水至淹没长颈漏斗下端管口,继续注入少量水,至漏斗颈部形成水柱,静置,观察水柱是否下降(或关闭弹簧夹,从长颈漏斗中缓缓注水至淹没长颈漏斗下端管口,用热水加热试管,观察长颈漏斗颈部是否有液柱上升)
(3)2Al+6HCl=2AlCl3+3H2↑
(4)向下排空气法(或排水法)
(5)<;铝比锌金属活动性强
