问题
填空题
如图所示2套实验装置,分别回答下列问题。
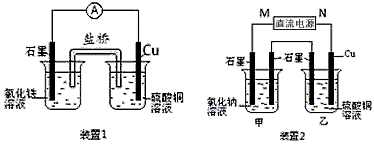
(1)装置1中的Cu是________极(填“正”或“负”),该装置发生的总反应的离子方程式为________________________。
(2)装置2中甲烧杯盛放100 mL 0.2 mol/L的NaCl溶液,乙烧杯盛放100 mL 0.5 mol/L的CuSO4溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞,观察到右边石墨电极附近首先变红,左边石墨电极附近无明显现象。
① 电源的M端为_______极,甲烧杯右边石墨电极附近首先变红的原因是________________。
② 乙烧杯中电解反应的离子方程式为________________________。
③ 若装置甲阴、阳两极各产生112mL气体(标准状况),则装置乙所得溶液的pH为________(忽略反应前后溶液的体积变化)。
答案
(1)负;2Fe3++Cu===2Fe2++Cu2+
(2)①正;H2O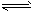 H++OH-,H++2e-===H2↑,c(OH-)>c(H+),溶液呈碱性;
H++OH-,H++2e-===H2↑,c(OH-)>c(H+),溶液呈碱性;
②2Cu2++ 2H2O 2Cu + O2↑ + 4H+;③1
2Cu + O2↑ + 4H+;③1
