(1)在298K时,1molC2H6在氧气中完全燃烧生成二氧化碳和液态水,放出热量1558.3 kJ。写出该反应的热化学方程式______________________。
(2)利用该反应设计一个燃料电池:用氢氧化钾溶液作电解质溶液,多孔石墨做电极,在电极上分别通入乙烷和氧气。通入乙烷气体的电极应为_______极(填写“正”或“负”),该电极上发生的电极反应是________________(填字母代号)。
a. 2C2H6-14e-+7O2 === 4CO2 + 6H2O b. C2H6-14e-+18OH- === 2CO32-+12H2O
c. O2+2H2O+4e- === 4OH- d. O2-4e-+4H+ === 2H2O
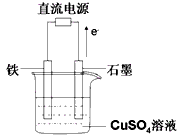
(3)在下图所示实验装置中,石墨棒上的电极反应式为_________________;如果起始时盛有1000mLpH=5的硫酸铜溶液(25℃,CuSO4足量),一段时间后溶液的pH变为1,此时可观察到的现象是__________________;若要使溶液恢复到起始浓度(温度不变,忽略溶液体积的变化),可向溶液中加入_________(填物质名称),其质量约为__________________。
(1)2C2H6(g)+ 7O2(g)=== 4CO2(g)+ 6 H2O(l) △H=-3116.6 kJ/mol
(2)负;b
(3)4OH-- 4e- === O2↑+ 2H2O;石墨电极表面有气泡产生,铁电极上附着一层红色物质,溶液颜色变浅
; 氧化铜(或碳酸铜);4g(或6.2g)
