问题
计算题
工业上用煅烧石灰石(主要成分为CaCO3)制取生石灰.
(1)碳酸钙中钙元素的质量分数是 _________ .
(2)某工厂用12t含碳酸钙为75%的石灰石,其中所含碳酸钙的质量是 _________ t.
(3)上述石灰石理论上可以制得生石灰多少t?
答案
解:
(1)40%
(2)9
(3)设生成氧化钙的质量为x
CaCO3 CaO+CO2↑
CaO+CO2↑
100 56
9t x
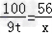
解之得:x=5.04g
因为生成的生石灰中含有未参与反应的杂质,杂质的质量=12t×(1﹣75%)=3t
所以最终可以生产生石灰的质量=5.04t+3t=8.04t
答:可生产生石灰8.04吨.
