问题
选择题
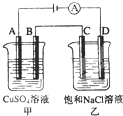
如图两个电解槽中,A、B、C、D均为石墨电极.若电解过程中共有0.02mol电子通过,下列叙述中正确的是( )
A.甲烧杯中A极上最多可析出铜0.64g
B.甲烧杯中B极上电极反应式4OH--4e-=2H2O+O2↑
C.烧杯中C极上电极反应式为4H++4e-=2H2↑
D.乙烧杯中滴入酚酞试液,D极附近先变红
答案
A.A极(阳极)反应式为4OH--4e-=2H2O+O2↑,生成氧气,不能析出铜,故A错误;
B.甲烧杯中B极上电极反应式为:Cu2++2e-=Cu,故B错误;
C.烧杯中C极上电极反应式为2Cl--2e-=Cl2↑,故C错误;
D.D极(阴极)反应式为2H++2e-=H2↑,由于H+放电,打破了水的电离平衡,导致D极附近溶液呈碱性(有NaOH生成),故D正确.
故选D.
