A、B、C三种强电解质,它们在水中电离出的离子如下表所示:
| 阳离子 | Na+、K+、Cu2+ | ||
| 阴离子 | SO
|
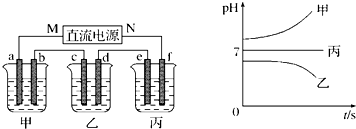
(1)M为电源的______极(填写“正”或“负”);电极b上发生的电极反应式为______.
(2)计算电极e上生成的气体在标准状况下的体积______.
(3)写出乙烧杯中发生电解的总反应化学方程式______.
(4)如果电解过程中B溶液中的金属离子全部析出,此时电解能否继续进行______(填写“能”或“否”)原因为______.
(5)此时要使丙中溶液恢复到原来的状态,操作是______.
测得乙中c电极质量增加了16g,则乙中含有Cu2+,结合离子的共存可知,B为CuSO4,丙中pH不变,则C为硫酸钠或硫酸钾,甲中pH增大,则A为KOH或NaOH,
(1)乙中c电极铜离子得电子,则c为阴极,即M为电源负极,则b为阳极,碱溶液中OH-放电,电极反应为4OH--4e-=O2↑+2H2O,故答案为:负;4OH--4e-=O2↑+2H2O;
(2)e电极上氢离子放电生成氢气,n(Cu)=
=0.25mol,由Cu~2e-~H2↑可知生成标况下氢气的体积为0.25mol×22.4L/mol=5.6L,故答案为:5.6L;16g 64g/mol
(3)乙烧杯中为惰性电极电解硫酸铜溶液,总反应为2CuSO4+2H2O
2Cu+O2↑+2H2SO4, 电解 .
故答案为:2CuSO4+2H2O
2Cu+O2↑+2H2SO4; 电解 .
(4)B溶液中的金属离子全部析出,电解质为硫酸,电解时溶液中的氢离子、氢氧根离子放电,能继续电解,
故答案为:能;电解硫酸溶液;
(5)丙中电解质为硫酸钠或硫酸钾,实质为电解水,由电子守恒可知H2O~2e-~Cu,则要恢复原状,加0.25mol×18g/mol=4.5g水,故答案为:加入4.5g水.
