问题
选择题
早在1807年化学家戴维用电解熔融氢氧化钠制得钠 4NaOH(熔)
4Na+O2↑+2H2O;后来盖•吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为:3Fe+4NaOH 电解
Fe3O4+2H2↑十4Na↑.下列有关说法正确的是( )1100℃
A.电解熔融氢氧化钠制钠,阳极发生电极反应为:2OH--2e-=H2↑+O2↑
B.盖•吕萨克法制钠原理是利用铁的还原性比钠强
C.若戴维法与盖•吕萨克法制得等量的钠,则两反应中转移的电子总数也相同
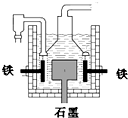
D.目前工业上常用电解熔融氯化钠法制钠(如图),电解槽中石墨极为阳极,铁为阴极
答案
A.由4NaOH(熔)
4Na+O2↑+2H2O可知,阳极氢氧根离子放电生成氧气和水,电极反应为4OH--4e-=2H2O+O2↑,故A错误; 电解 .
B.1100℃时生成Na蒸气,有利于反应正向移动,但Na的还原性大于Fe,故B错误;
C.由4NaOH(熔)
4Na+O2↑+2H2O、3Fe+4NaOH 电解 .
Fe3O4+2H2↑十4Na↑可知,戴维法生成4molNa转移4mol电子,但盖•吕萨克法生成4molNa转移8mol电子,则转移电子不等,故C错误; 电解 .
D.石墨极为阳极,氯离子放电,在阴极钠离子放电,发生2NaCl
2Na+Cl2↑,故D正确; 电解 .
故选D.

