用如图装置(X、Y是直流电源的两极)分别进行下列各组实验,则下表中所列各项对应关系均正确的一组是( )
| 选项 | 电源X极 | 实验前U形管中液体 | 通电后现象及结论 |
| A | 正极 | Na2SO4溶液 | U形管两端滴入酚酞后, a管中呈红色 |
| B | 正极 | AgNO3溶液 | b管中电极反应式是4OH-4e-=2H2O+O2↑ |
| C | 负极 | KCl和CuCl2混合溶液 | 相同条件下,a、b两管中产生的气体总体积可能相等 |
| D | 负极 | AlCl3溶液 | a管中先产生白色沉淀后沉淀溶解 |
A.A
B.B
C.C
D.D
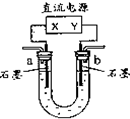
A、电源X极为正极,a管中石墨电极为阳极,b管中石墨电极为阴极,电解硫酸钠溶液的实质是电解水,H+在阴极区放电,OH-在阳极区放电,故在阴极区有大量的OH-,滴入酚酞后,b管中呈红色,在阳极区有大量的H+,a管中呈无色,故A错误;
B、电解硝酸银,Ag+在阴极放电,电极反应式为:4Ag++4e-=4Ag,OH-在阳极反应:4OH-+4e-=2H2O+O2↑,即b管中电极反应是析出金属银的反应,故B错误;
C、电解KCl和CuCl2混合溶液时,当X为负极时,则a管中产生的气体是氢气,氢离子在铜离子放电完毕之后放电,b管中产生的气体是氯气,氯离子放电完毕之前,生成氢气少,氯气多,此后为电解水,2H2O
2H2↑+O2↑,生成的氧气多,氢气少,电解一定的水,可以使两管中产生的气体总体积相等,故C正确; 电解 .
D、电源X极为负极,a管中石墨电极为阴极,b管中石墨电极为阳极,a管中氢离子放电,生成OH-,与铝离子反应生成氢氧化铝沉淀,氯离子放电完毕,为电解水,氢氧化铝沉淀在最低部,整个溶液为中性,氢氧化铝不溶解,故D错误;
故选C.

 L2
L2