NaClO溶液是一种常用的环境消毒液,某化学研究性学习小组查资料得到氯气和烧碱在温度700C以上主要发生副反应:3Cl2+6NaOH=NaClO3+5NaCl+3H2O,并设计了两套制备NaClO溶液的装置,如图所示:
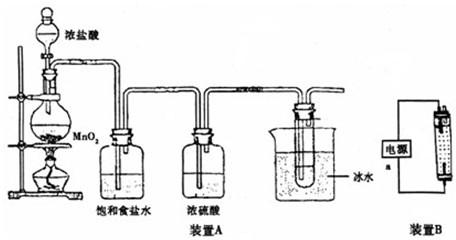
(Ⅰ)根据装置A回答:
(1)烧瓶内反应的化学方程式为______.大试管内反应的离子方程式为______.
(2)饱和食盐水的作用是______;能否省去盛浓硫酸的洗气瓶(填能或不能)______.装置A还需连一个怎样的装置?______.
(Ⅱ)根据装置B(电极均为石墨)回答:
(3)装置B中装的溶液是-______,a接电源的极______-;电解总化学的方程式为______.
(4)电解一段时间后(原电解质尚有利余)取电解液,滴至红色石蕊试纸上,观察到的现象是______.
(1)二氧化锰和浓盐酸反应制取氯气的原理为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,大试管中发生的反应是氯气和冷的氢氧化钠溶液反应,故答案为:MnO2+4HCl(浓) △ .
MnCl2+Cl2↑+2H2O;Cl2+2OH-=Cl-+ClO-+H2O; △ .
(2)饱和食盐水的作用是除去杂质气体HCl;氯气中的水蒸气不影响次氯酸钠的制取,所以氯气可以不干燥,但是氯气有毒,一定要进行尾气处理,故答案为:除去杂质气体HCl;能;尾气气吸收装置;
(3)制取次氯酸钠的原理是让氯气和氢氧化钠反应,氯气和氢氧化钠的产生来自饱和食盐水的电解,为了让产生的氯气被溶液全部吸收,氯气一定要在下面的电极上生成,故下面的电极上是氯离子失去电子的过程,为阳极,所以a极为电源的正极,故答案为:NaCl;正;NaCl+H2O
NaClO+H2↑; 通电 .
(4)电解一段时间后的电解液主要成分是次氯酸钠和氯化钠,次氯酸钠具有漂白性,水解显示碱性,滴加到红色石蕊试纸上以后会先变蓝后褪色,故答案为:先变蓝后褪色.

 是T形交叉路口标志。
是T形交叉路口标志。