按右图装置实验,用惰性电极电解足量的NaOH溶液和足量CuSO4溶液.通电一段时间后,c极上有6.4gCu析出.
(1)电源P为______极;
(2)b极产生气体的体积为______L(标准状况);
(3)A烧杯溶液PH变化______(增大、减小或不变 )
(4)d极上所发生的电极反应式______,B烧杯总反应的化学方程式______.若要使B中溶液恢复电解前的状态,可向溶液中加入______(填写物质的化学式)______g.
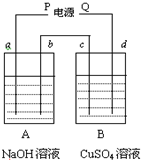
(1)B杯中c质量增加,说明Cu沉积在c电极上,所以c是阴极,d是阳极,即Q为正极,P为负极,故答案为:负;
(2)P是负极,所以a是阴极,b是阳极,b极上的电极反应为:4OH--4e-=2H2O+O2↑,c极上的电极反应为:Cu2++2e-=Cu,整个电路是串联的,所以每个烧杯中的电极上转移电子数是相等的,据电极反应:Cu2++2e-=Cu,可知c极上有6.4gCu析出,转移0.2mol电子,当转移0.2mol电子时,b极上生成氧气的物质的量为0.05mol,体积为0.05mol×22.4L/mol=1.12L.故答案为:1.12;
(3)A烧杯溶液电解的实质是电解水,所以氢氧化钠溶度增大,PH变大,故答案为:增大;
(4)d是阳极,电解硫酸铜时,在阳极上是氢氧根离子放电,电极反应式为:4OH--4e-=2H2O+O2↑,总的电解原理方程式为:2CuSO4+2H2O
2Cu+O2↑+2H2SO4,根据电解质复原出什么加什么的原则,则需要接入氧化铜或是碳酸铜,知c极上有6.4gCu析出时,即0.1mol铜析出时,要加入氧化铜或是碳酸铜均是0.1mol,质量分别是8g和12.4g, 通电 .
故答案为:4OH--4e-=2H2O+O2↑;2CuSO4+2H2O
2Cu+O2↑+2H2SO4;CuO (或CuCO3); 8(或12.4). 通电 .