如图装置实验,A、B两烧杯分别盛放200g10%NaOH和足量CuSO4溶液.通电一段时间后,c极上有Cu析出,又测得A杯中溶液的质量减少4.5g(不考虑水的蒸发).
请回答下列问题:
(1)电源P极为______极;请分别写出b极和c极上发生的电极反应式:______;______
(2)c极上析出固体铜的质量为______g
(3)若装置中用铅蓄电池作电源,已知铅蓄电池放电时发生如下反应:
负极:Pb+SO42-=PbSO4+2e-
正极:PbO2+4H++SO42-+2e-=PbSO4+2H2O
假设在a极制得气体0.050mol,这时电池内消耗的H2SO4的物质的量至少是______mol.
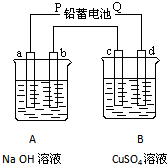
(1)c极上有Cu析出,说明c为电解池的阴极,d为阳极,则P为负极,b为电解NaOH溶液的阳极发生反应为4OH--4e-=2H2O+O2↑,c为电解硫酸铜溶液的阴极,发生反应为Cu2++2e-=Cu,
故答案为:负;4OH--4e-=2H2O+O2↑;Cu2++2e-=Cu;
(2)A总反应式为2H2O
2H2↑+O2↑,A杯中溶液的质量减少4.5g,应为电解的水的质量,n(H2O)= 电解 .
=0.25mol,转移电子为0.5mol,c极上析出固体铜的物质的量为0.25mol,质量为0.25mol×64g/mol=16g,4.5g 18g/mol
故答案为:16;
(3)a极制得气体0.050mol,因为氢气,转移电子0.10mol,铅蓄电池总反应式为Pb+PbO2+2H2SO4=2PbSO4+2H2O,则电池内消耗的H2SO4的物质的量至少是0.10mol,
故答案为:0.10.
