已知pH为4~5的条件下,Cu2+几乎不水解,而Fe3+几乎完全水解.某学生用电解纯净的CuSO4溶液的方法,并根据电极上析出Cu的质量(m)以及电极上产生气体的体积(V mL 标准状况)来测定Cu的相对原子质量,过程如下:
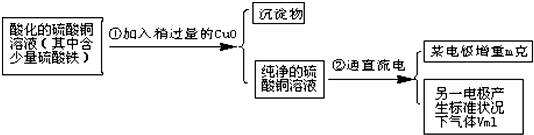
回答下列问题:
(1)加入CuO的作用是______.
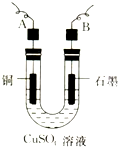
(2)步骤②中所用的部分仪器如图所示,则A、B分别连直流电源的______极和______极
(填“正”或“负”).
(3)电解开始后,电解的离子方程式为______.
(4)下列实验操作中必要的是______(填写字母).
A.称量电解前的电极的质量;
B.电解后,电极在烘干称量前,必须用蒸馏水冲洗;
C.刮下电解后电极上析出的铜,并清洗,称量;
D.电解后烘干称重的操作中必须按“烘干→称量→再烘干→再称量”进行;
E.在有空气存在的情况下,烘干电极必须用低温烘干的方法.
(5)铜的相对原子质量为______(用带有m、V的计算式表示).
(1)pH为4~5的条件下,Cu2+几乎不水解,而Fe3+几乎完全水解,加入稍过量的CuO,可以得到纯净的硫酸铜溶液,故加入CuO通过消耗H+而调整溶液的pH使之升高,使Fe3+完全水解形成Fe(OH)3沉淀而除去,
故答案为:消耗H+而调整溶液的pH使之升高,使Fe3+完全水解形成Fe(OH)3沉淀而除去;
(2)电解生成Cu与氧气,故Cu电极连接电源的负极,石墨电极连接电源的正极,故A、B分别连直流电源的负极、正极,
故答案为:负;正;
(3)电解硫酸铜溶液生成Cu、氧气与硫酸,电解的离子方程式为:2Cu2++2H2O
2Cu↓+O2↑+4H+, 电解 .
故答案为:2Cu2++2H2O
2Cu↓+O2↑+4H+; 电解 .
(4)需要准确称量生成铜的质量,铜电极前后质量之差为生成的Cu的质量,Cu电解表面会附着离子,应清洗除去,由于铜与氧气发生反应,在空气存在情况下,应低温烘干,称量两次之差小于天平的感量,说明烘干,故需要进行ABDE操作,不需要进行C操作,
故答案为:A、B、D、E;
(5)VmL氧气的物质的量为
=V×10-3L 22.4L/mol
mol,令Cu的相对原子质量为Mr,根据电子转移守恒,则:V 22400
×2=m Mr
mol×4,解得Mr=V 22400
,11200m V
故答案为:
.11200m V
