问题
计算题
取KI溶液25.00 mL,向其中滴加0.400 mol/L的FeCl3溶液135.0 mL,I-完全反应生成I2:2I-+2Fe3+====I2+2Fe2+。将反应后的溶液用CCl4萃取后分液,向分出的水溶液中通入Cl2至0.02500 mol时,Fe2+恰好完全反应。求KI溶液中KI的物质的量浓度。
答案
2.000 mol·L-1
KI与0.400 mol·L-1的FeCl3溶液135.0 mL反应,I-完全反应生成I2。由反应方程式:
2I-+2Fe3+====2Fe2++I2
2Fe2++Cl2====2Fe3++2Cl-
得反应的关系式为:
2I- — 2Fe2+ —Cl2
2 mol 1 mol
n(I-) 0.025 00 mol
n(I-)=2×0.025 00 mol="0.050" 00 mol
c(KI)=c(I-)=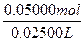 ="2.000" mol·L-1
="2.000" mol·L-1
