工业上采用如图所示电解装置制取活泼金属铝,由于阳极产生的氧气全部与石墨电极反应生成CO和CO2气体,因此在电解过程中碳电极需要不断补充.已知电解总反应方程式为:2Al2O3
4Al+3O2↑.通电 .
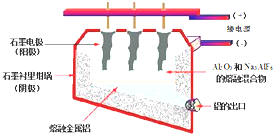
(1)阴极反应式为______;阳极反应式为______.
(2)若生产中每生成agAl,阳极损失石墨bg,则理论上产生CO和CO2的物质的量分别是______.
(3)对金属制品进行抗腐蚀处理,可延长其使用寿命.以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极电极反应式为______.
(1)根据电解方程式可知阴极生成Al,电极方程式为4Al3++12e-=4Al,阳极生成O2,电极方程式为6O2--12e-=3O2↑,
故答案为:4Al3++12e-=4Al;6O2--12e-=3O2↑;
(2)n(Al)=
mol,则转移电子a 27
mol×3=a 27
mol,消耗n(C)=a 9
mol,设生成xmolCO,ymolCO2,b 12
则
,x+y= b 12 2x+4y= a 9
解之得x=
mol,y=3b-a 18
mol,2a-3b 36
故答案为:CO:
mol、CO2:3b-a 18
mol;2a-3b 36
(3)阳极Al被氧化生成Al2O3,电解质溶液呈酸性,则阳极反应式为2Al+3H2O=Al2O3+6H++6e-,
故答案为:2Al+3H2O=Al2O3+6H++6e-.
