问题
选择题
.在25℃时,将两个铜电极插入一定质量的硫酸钠的饱和溶液中进行电解。通电一段时间后,阴极是逸出a mol气体,同时有Wg Na2SO4·10H2O晶体析出。若温度不变,剩余溶液中溶质的质量分数为( );若用铂电极电解硫酸钠的饱和溶液,则剩余溶液中溶质的质量分数为( )
A.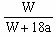 ×100%
×100%
B.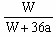 ×100%
×100%
C.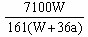 ×100%
×100%
D.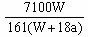 ×100%
×100%
答案
C; D。
若用铜电极电解时发生的电极反应:阳极为Cu→Cu2++2e-,阴极为2H++2e- →
H2↑,总的反应式为:Cu + 2H2O  Cu(OH)2↓+H2↑。阴极逸出a mol H2,水被电解了2a mol。而依据溶解度的知识,电解的水与析出的Wg Na2SO4·10H2O晶体应组成该温度下的饱和溶液,故,剩余溶液中溶质的质量分数与电解的水和析出的Wg Na2SO4·10H2O晶体应组成该温度下的饱和溶液质量分数相等,即:
Cu(OH)2↓+H2↑。阴极逸出a mol H2,水被电解了2a mol。而依据溶解度的知识,电解的水与析出的Wg Na2SO4·10H2O晶体应组成该温度下的饱和溶液,故,剩余溶液中溶质的质量分数与电解的水和析出的Wg Na2SO4·10H2O晶体应组成该温度下的饱和溶液质量分数相等,即: ×100% =
×100% = % ;若用铂电极电解时发生的总的反应式为:2H2O
% ;若用铂电极电解时发生的总的反应式为:2H2O  O2↑+ 2H2↑,阴极逸出a mol H2,水被电解了a mol,则剩余溶液中溶质的质量分数为:
O2↑+ 2H2↑,阴极逸出a mol H2,水被电解了a mol,则剩余溶液中溶质的质量分数为: ×100% =
×100% = %。
%。
