问题
选择题
某同学按如图所示的装置进行实验,A、B为常见金属,它们的硫酸盐可溶于水。当K闭合后,在交换膜处SO42-从右向左移动。下列分析不正确的是
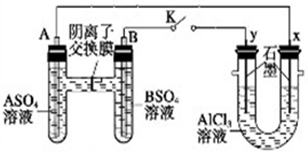
A、溶液中c(A2+)增大
B、B的电极反应:B2++2e-=B
C、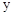 电极上有Cl2产生,发生氧化反应
电极上有Cl2产生,发生氧化反应
D、右边装置反应的离子方程式为:2Cl-+2H2O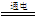 H2↑+Cl2↑+2OH-
H2↑+Cl2↑+2OH-
答案
答案:D
左部分为原电池,阴离子SO42-从右向左移动,说明A极为负极:A—2e-=A2+,A正确;B为正极:B2++2e-=B,B正确
x、y极分别联接外电源的负极与正极,故:
x电极为阴极:2H2O+2e-=H2↑+2OH-,Al3++3OH-=Al(OH)3↓,D不正确
y电极为阳极:2Cl-—2e-=Cl2↑,氧化反应,C正确
答案为D
