实验室中常采用分解过氧化氢(H2O2)溶液(用二氧化锰作催化剂)或加热高锰酸钾的方法制取氧气.请回答下列问题:
(1)图中标号仪器的名称:a______b______
(2)写出用上述两种方法制取氧气的任一个化学反应方程式______.
(3)用过氧化氢分解制取氧气的装置如图所示.
用该方法收集氧气时检验是否收集满的方法是______.
(4)如果反应器中反应很剧烈,应该采取的安全措施是______.
A.减慢液体的滴加速度 B.换用体积小的锥形瓶 C.加热锥形瓶
(5)与用高锰酸钾制取氧气相比,用过氧化氢制取氧气的优点是______(任写一点)
(6)MnO2是反应中的催化剂,可回收再利用.采用______方法,可从反应后的剩余物中分离出MnO2.
(7)若只改变装置中的药品,此套装置还可用以制取的气体是______,反应的化学方程式是______,常用______鉴定瓶中收集到的气体.
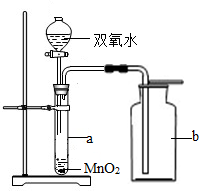
(1)做实验时,常常要用到酒精灯、试管、烧杯、铁架台等化学仪器,一定要了解并识记它们,故可知试管,集气瓶;
(2)由题意知,反应物双氧水,生成物水合氧气,反应条件为二氧化锰,故2H2O2
2H2O+O2↑; MnO2 .
(3)用向上排空气法收集氧气时,检验是否收集满的方法是将带火星的木条放在集气瓶口,观察是否复燃;
(4)如果反应器中反应很剧烈,应该采取的安全措施是:A减慢液体的滴加速度;;
(5)用高锰酸钾制取氧气,需要加热,会污染环境;而用过氧化氢制取氧气的优点是:不需要加热,节能、环保、安全;
(6)MnO2是反应中的催化剂,可回收再利用.采用过滤方法,可从反应后的剩余物中分离出MnO2;
(7)若只改变装置中的药品,此套装置没有加热装置,还可用以制取的气体是CO2或二氧化碳,利用大理石和稀盐酸反应制取二氧化碳,故化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑;二氧化碳用澄清石灰水验证.
故答为:(1)试管,集气瓶;(2)2H2O2
2H2O+O2↑或2KMnO4 MnO2 .
K2MnO4+MnO2+O2↑; △ .
(3)将带火星的木条放在集气瓶口,观察是否复燃;(4)A;(5)节能、环保、安全(答案合理即可)
(6)过滤;(7)CO2或二氧化碳;CaCO3+2HCl=CaCl2+H2O+CO2↑;澄清石灰水
