某校化学研究性学习小组探究气体制取的实验原理与方法.
(1)甲同学将课本的基础知识进行整理如下图,请你帮助他完成相关内容.
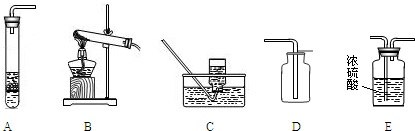
| 制取气体 | 所需药品 | 装置连接顺序 |
| 氧气 | 氯酸钾和二氧化锰 | BC/BD |
| 二氧化碳(干燥) | 大理石(石灰石)和稀盐酸 | AED |
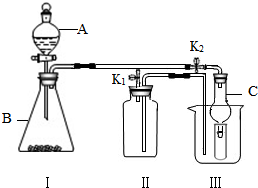
①大理石与稀盐酸反应制取二氧化碳 ②锌(固体)与稀硫酸反应制取氢气
(3)丙同学认为在不改变I、Ⅱ、Ⅲ装置的仪器及位置的前提下,该装置既可用于过氧化钠(Na2O2)与水反应制取氧气,另一产物为氢氧化钠,则该反应的化学方程式为:______.
(4)丁同学打开K2、关闭K1,利用I、Ⅲ装置来验证生成的二氧化碳,此时C中盛放的试剂是______,可以观察到的现象是______,反应的化学方程式为______.
若要证明二氧化碳与水发生反应,此时C中盛放的试剂是______.
(1)用氯酸钾和二氧化锰反应制取氧气需要加热反应,我们可选用B作为发生装置;又因氧气的密度大于空气的密度,并且不易溶于水,可选C或D作为收集装置;大理石与稀盐酸反应制取二氧化碳,是固液在常温下反应,可用装置A作为发生装置;二氧化碳密度大于空气的密度,易溶于水,我们用装置D收集;又因为要收集干燥的二氧化碳,所以要在AD之间连接装置E.
(2)根据装置I、Ⅱ的导管进出口顺序可知,装置Ⅱ只能用来收集难溶于水或密度比空气小的气体,因此利用装置I、Ⅱ可收集H2.故选②;
(3)反应物是过氧化钠(Na2O2)与水,生成物是氧气和氢氧化钠,此反应的化学式是:2Na2O2+2H2O═4NaOH+O2↑;
(4)根据二氧化碳的特性进行分析;二氧化碳的特性是:能使澄清石灰水变浑浊;其溶液呈酸性,能使紫色石蕊试液变红.
故答案是:
(1)
| 制取气体 | 所需药品 | 装置连接顺序 |
| 氧气 | 氯酸钾和二氧化锰 | BC/BD |
| 二氧化碳(干燥) | 大理石(石灰石)和稀盐酸 | AED |
(3)2Na2O2+2H2O=4NaOH+O2↑;
(4)澄清石灰水,澄清石灰水变浑浊,Ca(OH)2+CO2=CaCO3↓+H2O,紫色石蕊试液.
