常温下,5%过氧化氢(H2O2)溶液中的过氧化氢在二氧化锰的催化作用下能迅速分解生成氧气和水.现有如图所示的实验装置(分液漏斗可以通过调节活塞控制液体的流速):
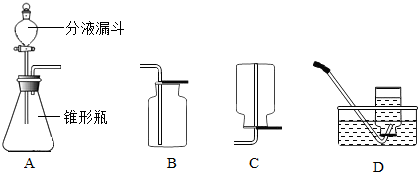
现用5%过氧化氢溶液制取氧气,请回答有关问题.
(1)分液漏斗中加入的物质是______,锥形瓶中加入的物质是______.
(2)写出该方法制取氧气的化学方程式:______.要收集一瓶纯净的氧气,应选择装置______.(填字母)
(3)某同学在观察到锥形瓶内产生大量气泡时,开始用B装置收集氧气,一段时间后,用带火星的木条伸入瓶口、瓶中、瓶底,都未见木条复燃,原因是:______
(4)若用此方法代替高锰酸钾加热制取氧气,其优点是______.(填字母)
A.生成物只有氧气 B.不需要加热 C.需加热.
(1)从长颈漏斗加入的药品是液体过氧化氢,锥形瓶中放的药品是固体二氧化锰,故填:5%过氧化氢溶液,二氧化锰;
(2)过氧化氢在二氧化锰的催化作用下能快速分解生成水和氧气,要收集纯净的氧气使用排水法,故填:2H2O2
2H2O+O2↑,D; MnO2 .
(3)装置漏气将会导致收集不到氧气,将带火星的木条插入集气瓶中各处不会出现木条复燃的情况,故填:实验装置气密性不好;
(4)利用过氧化氢制取氧气不需要加热,利用高锰酸钾制取氧气需要加热,故选:B.
