如图是李华同学设计的分解过氧化氢制取并收集氧气的装置图(①为分液漏斗,活塞可随时开关以控制液体滴加速度).请回答下列问题:
(1)仪器②的名称是______;
(2)MnO2的作用是______;实验后回收MnO2的方法是______;用化学方程式表示另外一种制取氧气的常用方法:______;
(3)检验氧气是否收集满的方法是______;
(4)用此装置还可以制取并收集的另外一种气体,写出反应的化学方程式:______.
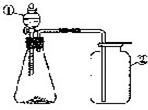
(1)依据实验室常用仪器的认识解决此题,②是集气瓶.答案为:集气瓶;
(2)二氧化锰在反应中既不参加反应,反应前后本身也不发生变化,只是改变了过氧化氢分解的速率,所以只是起催化剂的作用;二氧化锰不溶于水,因此实验完成后回收MnO2的操作为:先进行过滤,再洗涤干燥;实验室还可用加热氯酸钾的方法制取氧气,该反应的化学方程式是2KClO3
2KCl+3O2↑. 故答案为:催化作用;先进行过滤,再洗涤干燥;2KClO3MnO2 . △
2KCl+3O2↑;MnO2 . △
(3)因为氧气可以使带火星的木条复燃,所以可以将带火星的木条放在集气瓶口,若木条复燃,则证明收集满.
故答案为:将带火星的木条放在集气瓶口,若木条复燃,则证明收集满;
(4)此装置的发生装置属于固液在常温下反应,收集装置适用于密度比空气大的气体,因此用此装置还可以制取并收集二氧化碳气体,反应的化学方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑.故答案为:CaCO3+2HCl═CaCl2+H2O+CO2↑.
