(1)甲、乙同学分别用下图实验装置,使用二氧化锰固体与过氧化氢溶液在常温下作用制取氧气
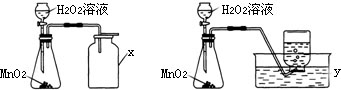
①写出上面装置中X、Y的仪器名称X______,Y______;
②从上述两个装置中,你能得出氧气的性质有:______;
③写出该实验制取氧气的化学方程式:______;
④用红砖粉末代替二氧化锰加入过氧化氢溶液中,也能够立即产生气泡,红砖粉末起______作用
(2)丙同学只用5% H2O2溶液加热制O2,用带火星的木条检验,木条很难复燃.同学们经过认真观察、讨论,制定了实验方案并进行实验:
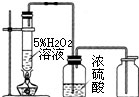
①第一组同学采取改变H2O2溶液质量分数的方法.用10%的H2O2溶液加热,反应一段时间后,用带火星的木条检验,木条复燃.
②第二组同学对实验装置进行改进,效果很好,如右图所示.用带火星的木条检验,也能使带火星的木条复燃.
从上面的实验结果中,你能得到的结论是:______.
(1)①X装置是集气瓶;Y装置是水槽;
②上述实验装置中氧气可用向上排空气法和排水法收集,故氧气密度大于空气,不易溶于水;
③过氧化氢在二氧化锰的催化作用下分解生成水和氧气,化学方程式为2H2O2
2H2O+O2↑; MnO2 .
④因为红砖粉末代替二氧化锰加入过氧化氢溶液中,也能够立即产生气泡,所以红砖粉末的作用是催化;
(2)用10%的H2O2溶液加热,溶液中的水经加热会有大量的水蒸气冒出,水蒸气会使带火星的木条温度降低,因此木条不复燃,而第二组同学加了浓硫酸干燥,故效果较好.
故答案为:(1)①集气瓶水槽(各1分) ②O2不易溶于水,密度比空气大(2分) ③2H2O2
2H2O+O2↑(2分) MnO2 .
④催化(2分)
(2)收集到的氧气含量(或浓度)不足或含有水蒸气时,不易使带火星的木条复燃(2分)
