问题
填空题
(14分)理论上讲,任何自发的氧化还原反应都可以设计成原电池。某同学利用 “Cu+2Ag+ =2 Ag +Cu2+ ” 反应设制一个化学电池,如图所示,已知该电池在外电路中,电流从a极流向b极。请回答下列问题:
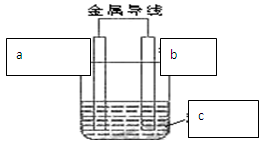
(1)b极是电池的 极,材料是 ,该极上出现的现象是 ,写出该电极的反应式 。
(2)a可能为
A、铜 B、银 C、铁 D、石墨
(3)c溶液是
A、CuSO4溶液 B、AgNO3溶液 C、酒精溶液
(4)若该反应过程中有0.2mol电子发生转移,则生成Ag为 克。
答案
(1)负、Cu、铜片逐渐溶解,溶液变蓝色、Cu – 2e- = Cu2+
(2) BD (3)B (4)21.6
由Cu+2Ag+ =2 Ag +Cu2+知,铜失电子,Cu – 2e- = Cu2+,做负极,不断溶解。正极材料应为比铜活性差的电极。
