(8分)某化学研究小组以铜为电极电解饱和食盐水,探究过程如下:
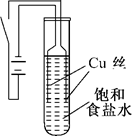
实验1:如图所示连接装置,电源接通后,与电池负极相连的铜丝上有大量气泡产生;与电池正极相连的铜丝由粗变细.电解开始30 s内,阳极附近出现白色浑浊,然后开始出现橙黄色浑浊,此时测定溶液的pH约为10.随着沉淀量的逐渐增加,橙黄色沉淀慢慢聚集在试管底部,溶液始终未出现蓝色.
实验2:将实验1中试管底部的橙黄色沉淀取出,分装在两支小试管中,以后的操作和现象如下:
| 序号 | 操作 | 现象 |
| ① | 滴入稀硝酸溶液 | 沉淀溶解,有无色气泡产生,最终得到蓝色溶液 |
| ② | 滴入稀硫酸溶液 | 橙黄色沉淀转变为紫红色不溶物,溶液呈现蓝色 |
| 物质 | 颜色 | 物质 | 颜色 |
| 氯化铜 | 固体呈棕色,浓溶液呈绿色,稀溶液呈蓝色 | 氢氧化亚铜(不稳定) | 橙黄色 |
| 碱式氯化铜 | 绿色 | 氢氧化铜 | 蓝色 |
| 氧化亚铜 | 砖红色或橙黄色 | 氯化亚铜 | 白色 |
(1)铜的常见正化合价为________、________,最终试管底部橙黄色沉淀的化学式________________.
(2)阴极上发生的反应为________________;阳极上发生的反应为________________.
(3)写出实验2中①、②的离子方程式:
①____________________________________,②______________________________.
(1)+1 +2 Cu2O (2)2H++2e-===H2↑
Cu+Cl--e-===CuCl↓(或Cu+OH--e-===CuOH↓)
(3)①3Cu2O+14H++2NO===6Cu2++2NO↑+7H2O
②Cu2O+2H+===Cu+Cu2++H2O
(1)铜有+1价和+2价,据实验1的现象说明橙黄色沉淀较稳定,再结合铜的化合物的颜色知该物质应为Cu2O,而Cu2O也符合实验2中的要求。
(2)在阴极上H+放电,反应为2H++2e-===H2↑,而阳极为铜,据现象及信息知反应为Cu-e-+Cl-===CuCl↓。
(3)Cu2O与稀HNO3发生了氧化还原反应,方程式为
3Cu2O+14H++2NO===6Cu2++2NO↑+7H2O,Cu2O与H2SO4反应,据反应现象知产物有CuSO4与Cu生成,故反应为Cu2O+2H+===Cu+Cu2++H2O。
