问题
选择题
常温下用惰性电极电解1L足量KCl的溶液,若通过n mol电子的电量,则溶液的pH与n的关系是(设电解前后溶液的体积不变)( )
A.pH=n
B.pH=-lg n
C.pH=14-lgn
D.pH=lgn+14
答案
答案:D
根据方程式2KCl+2H2O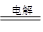 2KOH+H2↑+↑Cl2↑可知,如果转移nmol电子,则生成nmol氢氧化钾,所以氢氧化钾的浓度是nmol/L,则氢离子浓度是
2KOH+H2↑+↑Cl2↑可知,如果转移nmol电子,则生成nmol氢氧化钾,所以氢氧化钾的浓度是nmol/L,则氢离子浓度是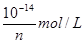 ,所以溶液的pH=lgn+14,答案选D。
,所以溶液的pH=lgn+14,答案选D。

 模型的厚度要求为()
模型的厚度要求为()