现有如图所示的下列实验装置.回答问题:
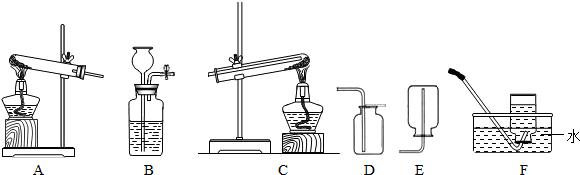
(1)检验B装置气密性方法是______.
(2)如果用高锰酸钾来制取干燥的氧气,反应方程式为______;可选用的发生装置和收集装置是_______ (填写序号).
(3)质量分数为3%的医用双氧水在常温下难分解;但在双氧水溶液中加入铁锈,就会迅速分解且反应结束后过滤出的铁锈可重复使用.试写出该反应的化学方程式______,选择气体发生装置的依据是______、______.
(4)某化学研究小组的同学欲对某种塑料袋的组成进行分析探究(资料显示该塑料只含C、H
两种元素),他们设计了如图所示的实验装置,使该塑料试样在纯氧中燃烧,观察实验现象,分析有关数据,推算元素含量.
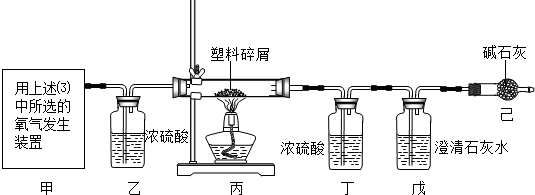
①仪器乙的作用是______,仪器戊中的现象是______.
②若仪器丙玻璃管中放入塑料试样为Wg,塑料试样充分燃烧后,仪器丁增重ag,则Wg该塑料试样中含氢元素的质量为______g(计算结果用分数形式表示).若装置中没有连接仪器乙,将使该塑料试样中氢元素的质量测算结果______(填“偏小”“偏大”、“无影响”).
(1)检查装置气密性的方法:先夹住弹簧夹,再向长颈漏斗中加水,形成液封后继续加水,长颈漏斗中会形成一段水柱,则气密性良好;
(2)制取氧气的反应装置和反应原理:固体+固体,且需要加热;认识常用仪器,写出加热高锰酸钾来制取干燥的氧气的反应方程式为:2KMnO4
K2MnO4+MnO2+O2↑;可选用的发生装置和收集装置是 A和D 或 A和F; △ .
(3)分解过氧化氢制取氧气,符合:固体+液体反应,不需加热;氧气密度大于空气,难溶于水; 选择发生装置的原理:根据反应物的状态和反应条件;双氧水在常温下加入铁锈分解制取氧气的反应方程式
为:2H2O2
2H2O+O2↑; 生锈 .
(4)过氧化氢在二氧化锰催化作用下产生氧气,放热,会有水蒸气生成;所以必须干燥,否则将使该塑料试样中氢元素的质量测算结果.
仪器丁增重ag,即为水的质量,则Wg该塑料试样中含氢元素的质量为:ag×
×100%=2 18
g;a 9
故答案为:(1)关闭止水夹,向长颈漏斗中加水形成液封后,继续加水,若长颈漏斗中有一段稳定的水注,则气密性良好;
(2)2KMnO4
K2MnO4+MnO2+O2↑;A和D 或 A和F; △ .
(3)2H2O2
2H2O+O2↑;反应物的状态;反应的条件; 生锈 .
(4)①干燥气体;澄清石灰水变浑浊;②
g;偏大.a 9