氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下:
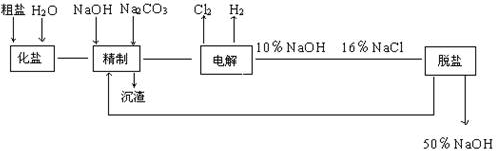
依据上图,完成下列填空:
(1)与电源负极相连的电极附近,溶液pH值(选填:不变、升高或下降),与电源正极相连的电极叫 极,检验该极上产物的方法是 。
(2)写出电解饱和食盐水的化学方程式 。
(3)如果粗盐中SO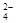 含量较高,必须添加钡式剂除去SO
含量较高,必须添加钡式剂除去SO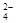 ,该钡试剂可以是(选填A.B.c,多选扣分)
,该钡试剂可以是(选填A.B.c,多选扣分)
A.Ba(OH)2 B.Ba(NO3)2 C.BaCl2
(4)判断钡试剂已经过量的方法是 。
(5)为有效除去Ca2+、Mg2+、SO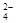 ,加入试剂的合理顺序为(选填a,b,c多选扣分)
,加入试剂的合理顺序为(选填a,b,c多选扣分)
A.先加NaOH溶液,后加Na2CO3溶液,再加钡试剂
B.先加NaOH溶液,后加钡试剂,再加Na2CO3溶液
C.先加钡试剂,后加NaOH溶液,再加Na2CO3溶液
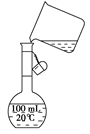
(6)为检验精盐纯度,需配制150 mL0.2 mol/LNaCl(精盐)溶液,下图是该同学转移溶液的示意图,图中的错误是 。
(1)升高 阳极 将淀粉碘化钾试纸用水润湿后粘在玻璃棒一端,靠近装有待测气体的集气瓶 如果黄绿色气体能使试纸变蓝色,证明含有Cl2。
(2)电解饱和食盐水的反应:2NaCl+2H2O  2NaOH+Cl2↑+H2↑
2NaOH+Cl2↑+H2↑
(3)C
(4)静止,向上层清液中继续滴加BaCl2,如不产生沉淀,已过量。
(5)B.C。
(6)未用玻璃棒引流 100 mL的容量瓶不能配制150 mL 溶液
题目分析:(1)与电源负极相连为阴极,生成氢气和NaOH,生成碱,所以pH升高;与正极相连为阳极,生成氯气;将淀粉碘化钾试纸用水润湿后粘在玻璃棒一端,靠近装有待测气体的集气瓶 如果黄绿色气体能使试纸变蓝色,证明含有Cl2。
(2)电解饱和食盐水的反应:2NaCl+2H2O  2NaOH+Cl2↑+H2↑
2NaOH+Cl2↑+H2↑
(3)添加钡试剂除去SO42-,注意不能引入新的杂质,选Ba(NO3)2会引入杂质硝酸根离子,所以该钡试剂不能选用。同理Ba(OH)2则引入了OH-离子。
(4)静止,向上层清液中继续滴加BaCl2,如不产生沉淀,已过量。
SO42-、Ca2+、Mg2+等分别与BaCl2溶液、Na2CO3溶液、NaOH溶液反应生成沉淀,可再通过过滤除去,Na2CO3溶液能除去过量的BaCl2溶液,盐酸能除去过量的Na2CO3溶液和NaOH溶液,所以应先加BaCl2溶液再加Na2CO3溶液,最后加入盐酸。故答案为:B.C。
(6)未用玻璃棒引流;100 mL的容量瓶不能配制150 mL 溶液。
