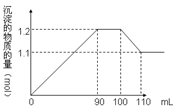
向100 mL BaCl2、AlCl3、FeCl3的混合液A中逐滴加入Na2SO4和NaOH的混合液B,产生沉淀的物质的量和加入溶液B的体积关系如图所示:则Na2SO4与FeCl3的物质的量浓度之比为
A.1︰1
B.10︰1
C.2︰1
D.5︰1
答案:B
正确答案:B
观察图:可得以下结论,
(1)加入B溶液110 mL时,Al(OH)3沉淀溶解完全,剩下沉淀BaSO4、Fe(OH)3。
(2)90—100 mL时这10 mL B溶液的滴加、Al(OH)3沉淀的溶解及BaSO4沉淀的生成同时发生: Ba2++SO42―=BaSO4↓,Al(OH)3+OH-=AlO2―+2H2O,并且物质的量相等,得出Na2SO4与NaOH的物质的量相等,即浓度相同。
(3)根据100—110 mL时B溶解Al(OH)3 0.01 mol,可得出90—110 mL时B溶解Al(OH)3 0.02 mol;又根据90—100 mL时这10 mL B溶液生成BaSO4 0.01 mol,所以总共有BaSO4为0.1 mol,最后Fe(OH)3为0.11 mol-0.1 mol="0.01" mol。
得出Na2SO4与FeCl3的物质的量浓度之比为(0.1mol/0.1L):(0.01mol/0.1L)=10:1,B选项正确。
附:各种物质的浓度如下表
| 溶质 | Na2SO4 | NaOH | BaCl2 | AlCl3 | FeCl3 |
| 浓度/mol·L-1 | 1 | 1 | 1 | 0.2 | 0.1 |
