对金属制品进行抗腐蚀处理,可延长其使用寿命。
(1)以下为铝材表面处理的一种方法:

①碱洗的目的是洗去铝材表面的自然氧化膜,碱洗时候常有气泡冒出,原因是 (用离子方程式表示)。
为将碱洗槽液中的铝以沉淀形式回收,最好向槽液中加入下列试剂中的 。
a.NH3 b.CO2 c. NaOH d.HNO3
②以铝材为阳极,在过量的H2SO4溶液中电解,铝材表面形成氧化膜,阳极电极反应式为 。取少量废电解液,加入NaHCO3溶液后产生气泡和白色沉淀,原因是 ; (用离子方程式表示)。
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨做阳极的原因是
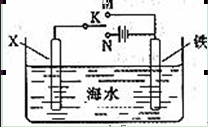
(3)利用下面的装置,可以模拟铁的电化学防护。若X为碳棒,为减缓铁的腐蚀,开关K应该置于 处。
若X为锌,开光K置于M处,该电化学防护法称为 。
(1)①2Al+2OH-+2H2O=2AlO2-+3H2↑(1分) b(1分)
②2Al-6e-+3H2O=Al2O3+6H+(2分)
HCO3-+ H+= CO2↑+ H2O (2分)
Al3++3HCO3-=Al(OH)3↓+3CO2↑(2分)
(2)补充溶液中消耗的Cu2+,保持溶液中Cu2+浓度恒定。(2分)
(3)N(1分);牺牲阳极的阴极保护法(或:牺牲阳极保护法)(1分)
题目分析:铝材碱性可以洗去油污,同时也可以洗去表面的氧化铝,裸露的铝会和碱溶液反应放出氢气,2Al+2OH-+2H2O=2AlO2-+3H2↑,氢氧化铝是两性氢氧化物,可溶于强酸强碱,因此,溶液中的偏铝酸根,应通入CO2使其沉淀成氢氧化铝,选b,②以铝材为阳极,在过量的H2SO4溶液中电解,铝材表面形成氧化膜,铝失电子发生氧化反应,阳极电极反应式为2Al-6e-+3H2O=Al2O3+6H+,取少量废电解液,加入NaHCO3溶液后产生气泡和白色沉淀,原因溶液中有硫酸,还有硫酸铝,HCO3-+ H+= CO2↑+ H2O,Al3++3HCO3-=Al(OH)3↓+3CO2↑,(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨做阳极的原因是补充溶液中消耗的Cu2+,保持溶液中Cu2+浓度恒定。(3)若X为碳棒,为减缓铁的腐蚀,应构成电解池,阴极的电保护法,开关K应该置于N处,若X为锌,开光K置于M处,该电化学防护法称为牺牲阳极的阴极保护法。
