问题
选择题
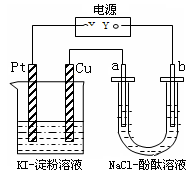
CuI是一种不溶于水的白色固体,它可以由反应: 2Cu2++4I-=2CuI↓+I2而得到.如图所示装置中,a、b都是惰性电极,通电一段时间后,在KI-淀粉溶液中阳极周围变蓝色,则下列说法正确的是
A.若a极变红,则在Pt电极上:2I--2e-=I2淀粉遇碘变蓝
B.若b极变红,在Pt电极上:4OH--4e-=2H2O+O2O2将I-氧化为I2,淀粉遇碘变蓝
C.若a极变红,在Cu电极上:Cu-2e-→Cu2+,2Cu2++4I-=2CuI↓+I2,一段时间后淀粉遇碘变蓝
D.若b极变红,在Cu极上:Cu-2e-═Cu2+,Cu2+显蓝色
答案
答案:C
题目分析:A、a极变红,说明a极有氢氧化钠生成,则a为阴极,Pt为阴极,在Pt电极上:2H++2e-=H2↑,错误;B、b极变红,说明b极有氢氧化钠生成,b为阴极,Pt为阳极,应发生: 2I--2e-=I2淀粉遇碘变蓝,错误;C、a极变红,Cu为阳极,Cu先失电子,进入溶液,再发生2Cu2++4I-=2CuI↓+I2淀粉遇碘变蓝,正确;D、b极变红,Cu为阴极,在Cu极上:2H++2e-=H2↑,错误,答案选C。
