如图所示是利用电化学降解法治理水中的硝酸盐污染,电解槽中间用质子交换膜隔开,污水放入II区,通电使转NO3-化为N2,下面说法不正确的是 ( )
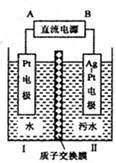
A.电解时H+从I区通过离子交换膜迁移到II区
B.Ag-Pt电极上发生发应:2 NO3-+10e-+6H2O= N2↑+12OH-
C.当电解过程中转移了1moL电子,则II区电解液质量减少2.8g
D.为增强溶液的导电性,I区水中可加入少量Na2SO4固体
答案:C
题目分析:A.由于污水放在II区,通电时污水中的NO3-得到电子转化为N2,所以与II区电极连接的电源B是负极,A是正极。根据同种电荷相互排斥,异种电荷相互吸引的原则,电解时H+从正电荷较多的I区通过离子交换膜迁移到负电荷较多的II区。正确。B.在电解时,在阴极Ag-Pt电极上发生发应:2 NO3-+10e-+6H2O= N2↑+12OH- 。正确。C.当电解时,在II区发生反应:42 NO3-+10e-+6H2O= N2↑+12OH- ,转移电子10mol,放出N2气体28g,使溶液减轻28g,同时有10mol的H+移向II区,质量又增加10g.总减轻18g.所以当电解过程中转移了1moL电子,则II区电解液质量减少1.8g.错误。D.由于在I区是OH-放电,所以为增强溶液的导电性,I区水中可加入少量Na2SO4固体。正确。