(1)下图是实验室制备物质、探究物质性质的常用装置,请回答:
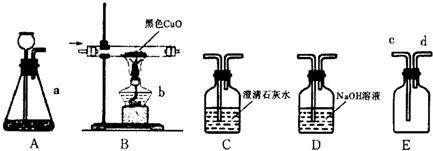
①仪器a、b的名称分别是______;
②连接装置A、E可用来制取氧气,装置A应与E的______端连接,反应的化学方程式为______;
③除去CO中少量的CO2,最好将气体通过装置______,理由是______;
④连接装置B、C可用来验证CO的还原性,CO通过装置B时可以看到______;装置C中出现白色浑浊,那么,装置B中发生反应的化学方程式______.
(2)课外学习小组为进一步探究活泼金属与酸反应的情况,做了以下两组对比实验(见下图).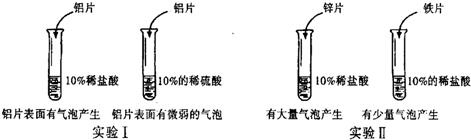
请分析实验Ⅰ、Ⅱ后回答:①实验Ⅰ反映了同种金属跟不同酸反应的剧烈程度不同;实验Ⅱ则表明了______剧烈程度不同,原因是______;
②按照实验Ⅰ和Ⅱ设计思路,请你再设计一组对比实验,简述实验方案.______.
(1)①图中仪器ab的名称分别是:锥形瓶、酒精灯.故答案为:锥形瓶、酒精灯;
②因为氧气的密度大于空气的密度,装置A应与E的c端连接;用装置A制取氧气时,是用二氧化锰作催化剂分解过氧化氢溶液的反应,反应的化学反应式是:2H2O2
2H2O+O2↑;故答案为:c、2H2O2MnO2 .
2H2O+O2↑;MnO2 .
③氢氧化钙微溶于水,氢氧化钠易溶于水,能配制浓溶液吸收二氧化碳效果好;故答案为:D、NaOH易溶于水;
④据题意和图示可知,此反应是一氧化碳还原氧化铜的反应,CO通过装置B时可以看到黑色粉末变红,反应化学式是:CO+CuO
Cu+CO2.故答案为:黑色粉末变红、CO+CuO△ .
Cu+CO2;△ .
(2)①两试管中酸的浓度相同,参加反应的金属不同.稀盐酸与锌片反应可生成大量气泡,与铁片反应可生成少量气泡.实验Ⅱ则表明了:不同种金属跟同一种酸反应的剧烈程度不同,原因是锌比铁活泼.故答案为:不同种金属跟同一种酸反应的、锌比铁活泼;
②同种金属,不同浓度的酸进行对比实验时,酸的浓度越大反应越快.故答案为:同种金属跟不同浓度的酸反应对比实验,浓度越大反应越快.(其他合理答案皆可)