问题
选择题
在由CH4和H2组成的混合气体中,测知碳元素的质量分数为60%,则混合气体充分燃烧生成二氧化碳和水的质量比为
A.11∶18
B.22∶9
C.1∶1
D.11∶27
答案
A
分析:假设混合气体中CH4和H2的质量分别为x,y,依据混合气体中碳元素的质量分数列出比例式,进行解答.然后利用质量守恒定律分别求出二氧化碳和水的质量.
解答:解:设混合气体中CH4质量为x,H2的质量为 y,可得
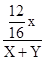 X100%=60%
X100%=60%
解得x:y=4:1
则气体中C、H元素质量比为:(4×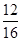 ):(4×
):(4×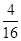 +1)=3:2
+1)=3:2
其中C、H原子个数比=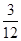 :
: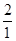 =1:8;所以二氧化碳和水的分子个数比为
=1:8;所以二氧化碳和水的分子个数比为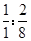 =1:4,二氧化碳和水的质量比为(1×44):(4×18)=11:18
=1:4,二氧化碳和水的质量比为(1×44):(4×18)=11:18
故选A