学习了实验室制取氧气之后,同学们对催化剂非常感兴趣,其他物质能否作过氧化氢分解的催化剂呢?于是利用课后时间来到实验室进行探究.
老师为他们准备的试剂有:5%的过氧化氢溶液、氧化铜、水.
同学们的实验设计如下,请你跟他们一起完成这个实验.
| 实验操作 | 实验现象 | 结论 | |
| 实验一 | ______ | 有少量气泡产生,木条不复燃 | 过氧化氢分解产生氧气,但是______. |
| 实验二 | 向盛水的试管中加入氧化铜,伸入带火星的木条 | 没有明显现象 | ______ |
| 实验三 | ______ | ______ | 氧化铜能加快加氧化氢的分解 |
(2)根据上面三个实验,同学们得出的实验结论是:氧化铜是过氧化氢分解的催化剂.
(3)小英同学认为仅由上述实验还不能完全得出 (2)中的结论,她的理由是:____、____.
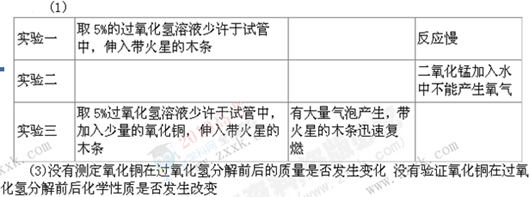
实验一:做实验时应先取少量溶液于试管中,因为要检验过氧化氢在常温下是否反应,反应速度快还是慢,所以应在试管中伸入带火星的小木条,根据现象木条不复燃说明过氧化氢反应很慢。实验二:向盛水的试管中加入氧化铜,伸入带火星的木条,没有明显现象,说明氧化铜加入水中不能产生氧气。实验三:验证过氧化氢中加入氧化铜后的反应速度,所以应取少量过氧化氢少许于试管中,加入少量氧化铜,伸入带火星的木条,可以看到有大量气泡产生,带火星的木条复燃。催化剂在反应前后性质不变,质量不变,所以要确认氧化铜在反应前后的质量性质是否发生变化,如果没有发生变化,才能肯定氧化铜时过氧化氢分解的催化剂。
