实验室制取气体所需装置如下图所示。
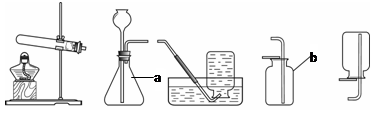
A B C D E
请回答以下问题:
(1)装置中标“a”“b”的仪器名称分别是_____ 、 。
(2)发生装置A与C连接制取氧气,当收集完氧气后,应先 ,再 。
(3)用装置B与 连接可以制取二氧化碳,检查装置B气密性的方法是____ .
(4)实验室可以用无水醋酸钠和碱石灰两种固态药品,经研磨均匀混合后装入反应装置中,加热产生甲烷气体。本实验可选用的气体发生装置为 (填字母序号),依据是
(5)把25g石灰石样品放入足量的稀盐酸中,石灰石中的碳酸钙与盐酸恰好完全反应(杂质不反应,也不溶解),生成气体的质量为8.8g。则石灰石中碳酸钙的质量分数为多少?
(1) 锥形瓶 集气瓶 (2分)
(2) 把导气管从水槽中拿出 熄灭酒精灯(2分)
(3) D(1分) 用弹簧夹夹住橡胶管,向长颈漏斗中注入水,若长颈漏斗中形成一段稳定的水柱,说明装置不漏气(2分)
(4) A (1分) 反应物是固体,反应需加热(2分)
(5) (6分)
解:设参加反应碳酸钙的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 8.8 g
100 :44=x:8.8 g
x= 20g
石灰石中碳酸钙的质量分数为:
20g/25g×100%=80%
答:石灰石中碳酸钙的质量分数为80%
分析:回顾实验室制取氧气和二氧化碳的原理、装置、实验步骤和注意事项对该题进行解答,以及利用根据化学方程式进行计算的步骤计算.
解答:解:(1)a、b是初中化学最常见的玻璃仪器;
(2)A是加热型的装置,制取氧气时为了防止水倒流炸裂试管,实验结束是先移除导管再熄灭酒精灯;
(3)二氧化碳密度大于空气,向上排空气法,选择D装置;检查装置B气密性,具体操作步骤:用弹簧夹夹住橡胶管,向长颈漏斗中注入水,若长颈漏斗中形成一段稳定的水柱,说明装置不漏气
(4)反应物是”无水醋酸钠和碱石灰两种固态药品”,条件是“加热”,则根据所学内容可知A装置可用制取甲烷;
(5)根据化学方程式计算步骤,一一进行解答即可;
故正确答案:
(1)锥形瓶;集气瓶
(2)把导气管从水槽中拿出 熄灭酒精灯
(3)D 用弹簧夹夹住橡胶管,向长颈漏斗中注入水,若长颈漏斗中形成一段稳定的水柱,说明装置不漏气
(4)A 反应物是固体,反应需加热
(5)解:设参加反应碳酸钙的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 8.8 g
100:44=x:8.8 g
x=20g
石灰石中碳酸钙的质量分数为:
20g/25g×100%=80%
答:石灰石中碳酸钙的质量分数为80%
