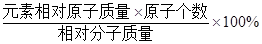问题
计算题
工业炼铁是把铁矿石和焦炭等原料一起加入高炉,在高温下通入空气进行一系列反应把铁还原出来。计算:
⑴Fe2O3的相对分子质量是: ;
⑵5000t含氧化铁84%的赤铁矿中,其氧化铁的质量是 t;
⑶上述赤铁矿理论上可炼得含铁98%的生铁 t。
答案
(1)160(1分);(2)4200t(1分);(3)3000t(1分)
题目分析:⑴Fe2O3的相对分子质量是:56×2+16×3=160;
⑵5000t含氧化铁84%的赤铁矿中,其氧化铁的质量是5000t×84%=4200t;
⑶上述赤铁矿理论上可炼得含铁98%的生铁的质量为(4200t×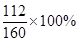 )/98%=3000t。
)/98%=3000t。
点评:相对分子质量是各元素相对原子质量的总和;
元素质量分数=