问题
问答题
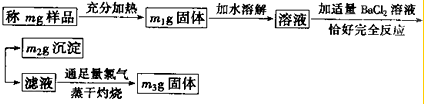
实验室需要纯净的氯化钾,现有氯化钾中含有少量溴化钾、硫酸钾和氯化铵.按照如图所示实验方案提纯分离出氯化钾:
列式计算该氯化钾样品中氯化铵、硫酸钾和溴化钾的质量分数.
其中氯化铵加热可分NH4Cl
NH3↑+HCl↑ △ .
氯气通入溴化钾溶液:Cl2+2KBr═2KCl+Br2.
答案
由图及物质的性质可知,充分加热时NH4Cl分解,则(m-m1)g为NH4Cl的质量,m2g为BaSO4的质量,由硫酸根离子守恒可计算硫酸钾的质量,m3g为KCl的质量,KCl来源于硫酸钾与氯化钡的反应生成及Cl2+2KBr═2KCl+Br2中反应生成,
则氯化铵的质量分数为
×100%=(m-m1)g mg
%,100(m-m1) mg
硫酸钾的质量分数为
×100%=(m2g×
)174 233 mg
%,100(m2×
)174 233 m
溴化钾的质量为[m1g-m2g×
-(m3g-m2g×174 233
)]×149 233
,238 149
则溴化钾的质量分数为
%,100(m1-
m2 -m3)×25 233 238 149 m
答:氯化钾样品中氯化铵、硫酸钾和溴化钾的质量分数分别为
%、100(m-m1) mg
%、100(m2×
)174 233 m
%.100(m1-
m2 -m3)×25 233 238 149 m
