三氯化铁在印刷、照像、医药、颜料以及有机合成催化剂方面有重要的应用。三氯化铁易潮解,在100℃时发生升华。通常,工业生产氯化铁有多种方法;其中一种常温氯化法是将氯气直接通入浸泡铁屑的水中来生成FeCl3。
请回答下列问题:
(1)完成常温氯化法制氯化铁过程中的化学反应方程式_____________(至少写出两个反应)。
(2)现对制备氯化铁的工艺进行改进,以废铁屑(含有SiO2、Al2O3、MgO、Fe2O3等杂质)为原料。其生产流程如图:
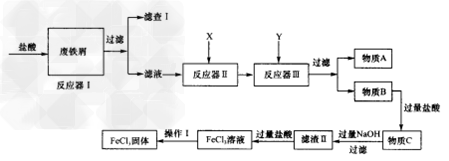
已知:氢氧化物沉淀过程中的pH:

KSPFe(OH)2=1×10-15
①X最好加入_________,写出相应的离子反应方程式_______________
A.KMnO4 B.FeCl3 C.H2O2 D.HNO3
②加入试剂Y的目的是调节pH的范围,试剂Y是____________。上表中a=__________。
(3)改进后的方法与前一种方法比较优点是_______________。
(4)实验室可以用下图所示装置制取无水三氯化铁。在实验开始时,A、B两个酒精应先点燃一会儿的是____________(填A或B),该装置应如何改进__________。

(1)① Cl2+H2O=HCl+HClO ;②2HCl+Fe=FeCl2+H2↑ ; ③2FeCl2+HClO+HCl=2FeCl3+H2O (2FeCl2+Cl2=2FeCl3 也可)
(2)①C ; H2O2+2Fe2+ +2H+=2Fe3+ +2H2O ;②Fe2O3 或Fe(OH)3 ; 9
(3)①过程中没有使用有毒的Cl2 ,绿色环保
②反应条件温和
③原料常见低廉
(4)A ;干燥管末端增加尾气处理装置
