根据下列装置图填写有关空格:
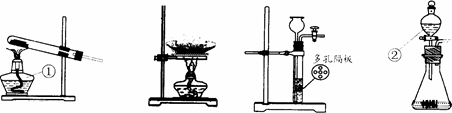
A B C D
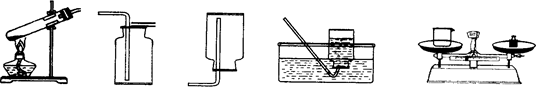
E F G H I
(1) 装置D中仪器②的名称为 。
(2) 实验室常用加热氯化铵与氢氧化钙固体混合物的方法制取氨气,同时得到氯化钙和水。通常情况下,氨气的密度比空气小且极易溶于水。若要制得干燥的氨气,则装置的连接顺序为_______(填装置的编号)反应的化学方程式_______________________________
(3) 除去粗盐中不溶性杂质的实验步骤是________________________________,用到的蒸发装置
是 。(填序号),还必须用下列玻璃仪器组合中的 (填序号)才能完成实验。
①漏斗、烧杯、玻璃棒 ②滴管、量筒、试管 ③集气瓶、表面皿、广口瓶
(4) 用氯化钠固体和水配制50克5%的氯化钠溶液,实验步骤____________________________。
若配制过程中,在已经有少量水的烧杯中加入5g氯化钠和95mL水,其他操作均规范,则所得溶液中氯化钠的质量分数_____________ (填“>”或“<”,或“=”)5%。
(1)分液漏斗
(2) AG 2NH4Cl+Ca(OH)2===CaCl2+2H2O+2NH3↑
(3) 溶解过滤蒸发 B ①
(4) 计算称量溶解 <
分析:(1)根据仪器的图形写出仪器的名称;
(2)根据制取氨气的反应物的状态、条件和氨气的溶解性、密度判断制取和收集装置,并写出化学方程式;
(3)粗盐提纯的步骤是溶解、蒸发、过滤;根据操作判断所用仪器;
(4)根据公式:溶液的溶质质量分数= ×100%计算判断.
×100%计算判断.
解答:解:(1)装置D中仪器②的名称为分液漏斗.
故答案为:分液漏斗;
(2)加热氯化铵与氢氧化钙固体混合物的方法制取氨气.是固固加热反应,我们可选用装置A作为发生装置;根据氨气密度比空气小且极易溶于水的性质可知,要用图中G向下排空气法收集.反应的化学方程式为 2NH4Cl+Ca(OH)2═CaCl2+2H2O+2NH3↑.
故答案为:AG;2NH4Cl+Ca(OH)2═CaCl2+2H2O+2NH3↑.
(3)要除去粗盐中不溶性杂质可以用过滤的方法,过滤前要先溶解;蒸发时可用酒精灯加热,蒸发皿作反应容器,还有铁架台,所以可以用装置B做反应容器;过滤、溶解、蒸发所用的玻璃仪器有:烧杯、漏斗、玻璃棒,故可选①.
故答案为:溶解、过滤、蒸发,B,①;
(4)用氯化钠固体和水配制5%的氯化钠溶液,要经过计算、称量、溶解几个步骤;根据公式:溶液的溶质质量分数= ×100%可知,在已经有少量水的烧杯中加入5g氯化钠和95mL水,则溶液的质量会偏大,故所得溶液中氯化钠的质量分数小于5%.
×100%可知,在已经有少量水的烧杯中加入5g氯化钠和95mL水,则溶液的质量会偏大,故所得溶液中氯化钠的质量分数小于5%.
故答案为:计算 称量 溶解;<.
