实验室中可以用右图装置来制取氧气

⑴写出该反应的化学方程式 ;在装药品前应首先进行 ;收集氧气的方法还可以用 。
⑵在实验室中该装置还可以用于制取的气体有 。写出该反应的化学方程式(只
写一个) 。
⑶上图装置中锥形瓶可用下图中的哪些仪器替代(填序号)

⑷某同学用了图7中的a、b、c、d、g、h仪器组装成氧气发生装置,请你推测该同学选用的化学药品是 。
⑸带火星的木条在盛过氧化氢溶液的试管中不能复燃,而在加热或加入二氧化锰后能复燃。请你归纳影响过氧化氢分解速率的因素有 等。你认为带火星的木条能否复燃与______有关。
⑴、⑵略 ⑶b、d ⑷高锰酸钾、温度、催化剂、氧气的体积分数(或浓度)
本题考查的是常用气体的发生装置和收集装置与选取方法,实验室制取氧气的反应原理,二氧化碳的实验室制法,以及正确书写化学方程式。
(1)由图可知,该装置属于“固液不加热型”,而又是利用它制取氧气,故知原料应是过氧化氢溶液,并用二氧化锰做催化剂,反应的化学方程式是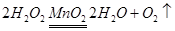 ,在装药品前应首先进行检查装置的气密性。又因为氧气的密度比空气大,还可用向上排空气法收集。
,在装药品前应首先进行检查装置的气密性。又因为氧气的密度比空气大,还可用向上排空气法收集。
(2)由于该装置属于“固液不加热型”,故还可以制取二氧化碳,化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑
(3)上图装置中锥形瓶只是一个反应容器,故可以用b、d来替代。
(4)用图中的a、b、c、d、g、h仪器组装成氧气发生装置,关键有h,即酒精灯,也就是要加热,故要么是加热高锰酸钾,要么是加热氯酸钾和二氧化锰的混合物。
(5)影响过氧化氢分解速率的因素有催化剂、温度以及溶液的浓度,因为浓度越大,反应速率越快,加热能加快过氧化氢的分解,有催化剂使分解速率加快;带火星的木条能否复燃与氧气的浓度有关,因为带火星的木条在空气中就不复燃。
