(7分)实验室常用一定质量分数的过氧化氢无色溶液(溶质为H2O2),在二氧化锰作催化剂的条件来制取氧气。某同学实验前测得过氧化氢溶液42.5g,加入1 g MnO2,完全反应后测得反应容器中剩余物质量为41.9g。 请回答:
(1)实验室用分解双氧水的方法制取氧气时,选择的发生装置应为_________。
(2)收集装置应选择_________,原因是____________________________________。
(3)反应后放出氧气的质量是多少,所用过氧化氢溶液中溶质的质量分数是多少?
[计算结果保留一位小数,计算过程按步骤写在答卷纸上]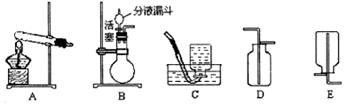
(1) B 。(2) C或D , 氧气不易溶于水且比空气的密度大 。
(3)[计算结果保留一位小数,计算过程按步骤写在答卷纸上]
解:①m氧气=" 42.5g" +1g -41.9g="1.6g" ............................... 1分
②设过氧化氢溶液中溶质的质量为X,则
2H2O2 ="=====" 2H2O + O2↑ .............................. 1分
68 32
X 1.6g
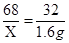 ∴X =3.4g..................... 1分
∴X =3.4g..................... 1分
∴过氧化氢溶液中溶质的质量分数="3.4g/42.5g" ×100%=8% ...... 1分
答:过氧化氢溶液中溶质的质量分数为8%
根据双氧水分解的反应原理及氧气的密度和溶解性确定发生和收集装置,并根据质量守恒定律判断氧气的质量,依据方程式和溶质的质量分数计算过氧化氢溶液中溶质的质量分数.
