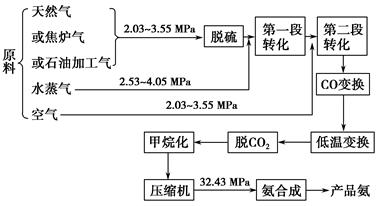
以合成氨工厂工艺流程如下图,试回答相关问题:
(1)不同的原料生产氢气其经济指标如下表:
| 天然气 | 石脑油 | 重油 | 煤焦 | |
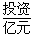 | 5.6 | 6.5 | 8.0 | - |
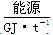 | 28~30 | 35.5 | 41.8 | 54.4 |
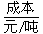 | 257 | 390~447 | 220~280 | 500 |
从上表数据及自然资源来看最具发展前景的是________。
A.天然气 B.石脑油 C.重油 D.煤焦
(2)脱硫工艺一般是通过金属氧化物来实现的,通过三步反应最后再生成金属氧化物,并得到单质硫,请补充第三步反应。
①MezOy+zH2S+(y-z)H2=MezSz+yH2O
②MezSz+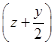 O2=MezOy+zSO2
O2=MezOy+zSO2
③__________________________________________________
(3)气体的精制 经净化过的气体仍有少量的CO等有害气体。常用的方法有铜洗法和甲烷化法。CO(g)+Cu(NH3)2Ac+NH3(l)[Cu(NH3)3CO]Ac;正反应放热,反应在铜洗塔中进行,吸收后的铜液送到再生器中,在再生器处解吸CO,适宜条件是________,解吸后铜液循环使用。甲烷化法则是把CO、CO2转化为对氨合成无害的CH4,主要反应是CO(g)+3H2(g) CH4(g)+H2O(g);正反应放热,甲烷化的条件是__________________。
CH4(g)+H2O(g);正反应放热,甲烷化的条件是__________________。

(4)500 ℃时,y随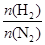 及压强的变化关系。纵坐标可能是____________,结合目前生产的条件,应控制的
及压强的变化关系。纵坐标可能是____________,结合目前生产的条件,应控制的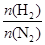 是________。
是________。
(1)A
(2)MezSz+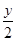 SO2=MezOy+
SO2=MezOy+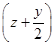 S
S
(3)减压和加热 高压、适当温度
(4)平衡时混合气体中氨气的体积分数 略小于3∶1
本题考查了平衡原理在工业生产中的应用。(1)发展前景一方面从成本比较,另一方面还要比较能量消耗,综合两者天然气更具前景。(2)补充方程式的关键是理解题意,最后生成金属氧化物和硫单质。反应②中生成SO2,要将SO2转化成硫单质。金属硫化物中硫显-2价,SO2中硫显+4价,通过两者归中反应可制得硫。(3)将CO解吸出来,要使平衡向逆反应方向移动,甲烷化的条件是平衡正向移动,高压和适宜温度。(4)压强增大,平衡向正反应方向移动,观察图像,y也增大;提高H2的比例,y先增大后减小,y可能是平衡时混合气体中氨气的体积分数。观察图像可知,当 略小于3∶1时,氨气的体积分数在相同条件下最大。
略小于3∶1时,氨气的体积分数在相同条件下最大。
