某研究性学习小组学习了工业“侯氏制碱法”的原理后:
[提出问题]能否在实验室模拟“侯氏制碱法”中制取NaHCO3的过程呢?
[实验原理]写出候氏制碱法反应的化学方程式为______.[实验验证]如图是该学习小组进行模拟实验时所用到的部分主要装置.
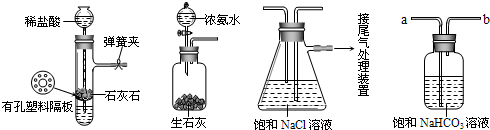
请回答下列问题:
(1)检验A装置气密性的方法是:塞紧带长颈漏斗的橡胶塞,夹紧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于试管内的水面,停止加水后,若______,说明装置不漏气.
(2)D是连接在装置A与装置C之间的气体净化装置,进气口是______(填a或b),D的作用是除去______气体.可否将瓶内试剂换为碳酸钠溶液______(填“可”“否”).
(3)实验时先向饱和NaCl溶液中通入较多的______,再通入足量的______,其原因是______.(填写序号)
①使CO2更易被吸收 ②NH3比CO2更易制取 ③CO2的密度比NH3大
(4)用______的方法将生成的NaHCO3晶体从混合物中分离出来.
如果要制得纯碱,还需发生的反应是(写出反应的化学方程式):______.
[得出结论]利用“侯氏制碱法”在实验室可以制取NaHCO3.
候氏制碱法是用二氧化碳通入氨化的饱和氯化钠溶液中反应生成碳酸氢钠晶体,反应的化学方程式:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl;
故答案为:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl
(1)随水的注入管内加压增大,漏斗内液体不能再流入试管,使长颈漏斗与管内液面出现液面差,并且液面差保持不变,说明装置气密性良好;
故答案为:长颈漏斗中注入水,漏斗中与试管中的液(水)面差保持不再变化或漏斗中的液(水)面不再下降;
(2)气体从a管通入时才能使气体通过溶液而达到净化气体的目的;装置D内盛放的碳酸氢钠溶液能与混在气体中的HCl发生反应生成氯化钠、水和二氧化碳,从而除去混在气体中的HCl;若换做碳酸钠溶液,二氧化碳也会被吸收;
故答案为:a;氯化氢(或HCl);否;
(3)先通入氨气,氨气与水形成呈碱性的氨水可与二氧化碳与水生成的碳酸发生反应,更有利于二氧化碳气体的吸收;
故答案为:NH3;CO2;①;
(4)通过过滤,可把混在溶液中的碳酸氢钠晶体分离出来;如果制得纯碱需要对碳酸氢钠固体加热分解得到,反应化学方程式为:2NaHCO3
Na2CO3+H2O+CO2↑ △ .
故答案为:过滤.2NaHCO3
Na2CO3+H2O+CO2↑ △ .
