问题
选择题
NA代表阿伏加德罗常数,下列叙述错误的是
A.10mL质量分数为98%的H2SO4,用水稀释至100mL,H2SO4的质量分数小于9.8%
B.在H2O2+Cl2 2HCl+O2反应中,每生成32g氧气,则转移2NA个电子
2HCl+O2反应中,每生成32g氧气,则转移2NA个电子
C.标准状况下,分子数为NA的CO、C2H4混合气体体积约为22.4L,质量为28g
D.NA个一氧化碳分子和0.5mol甲烷的质量比为7:2
答案
答案:A
A、硫酸溶液浓度越大,密度越大
设原溶液的密度为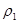 ,溶质的质量为m,则:
,溶质的质量为m,则: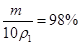 ,推出
,推出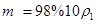 ;
;
设原溶液的密度为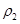 ,则其质量分数为:
,则其质量分数为: =
=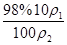 =9.8%×
=9.8%×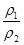 >9.8%
>9.8%
B、在H2O2+Cl2 2HCl+O2反应中,两个—1价氧升为0价,两个0价氯降至—1价,故有两个电子的转移。由方程式可看出,每生成32g氧气,则转移2NA个电子转移
2HCl+O2反应中,两个—1价氧升为0价,两个0价氯降至—1价,故有两个电子的转移。由方程式可看出,每生成32g氧气,则转移2NA个电子转移
C、CO、C2H4的摩尔质量相同,所以标准状况下,分子数为NA的CO、C2H4混合气体体积约为22.4L(阿伏加德罗定律适用于纯净或混合气体),质量为28g
D、NA个一氧化碳分子和0.5mol甲烷的质量比为28:8即7:2
故答案为A
