用NA表示阿伏加德罗常数,下列说法正确的是 ( )
①25℃时,PH=13的1.0L Ba(OH)2溶液中含有的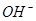 数目为0.2NA
数目为0.2NA
②1mol Na2O2与水完全反应时转移电子数为2 NA;
③6.8g熔融的KHSO4中含有的阳离子数为0.05 NA
④在标准状况下,22.4LSO3的物质的量为1mol;
⑤7.8g过氧化钠中含有的离子数为0.3 NA;
⑥由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2 NA
⑦200mL1mol/LFe2 (SO4) 3溶液中,Fe3+和SO42-离子数的总和是NA
⑧1mol FeCl3完全水解转化为氢氧化铁胶体后能生成NA个胶粒
⑨标准状况下,22.4LNO和11.2LO2混合后气体的分子总数为1.5 NA
⑩室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA
A.①③⑤⑥
B.③⑤⑥⑩
C.②④⑥⑦
D.③④⑤⑨
答案:B
说法①中,溶液OH-浓度应该依据PH值计算为0.1mol/L,再根据溶液体积计算OH-物质的量为0.1mol,最后数目应为0.1NA.说法②中,Na2O2是发生自身氧化还原反应,转移电子数为NA.说法④中,标准状况下,SO3不是气体状态.说法⑦中Fe3+要水解,使得溶液中Fe3+的离子数目小于0.4NA,最后与SO42-离子数目之和也小于NA.说法⑧中,胶粒是分子聚集体,一个Fe(OH)3胶粒是由多个Fe(OH)3聚集而成,所以1molFeCl3完全水解形成的胶粒数小于NA.说法⑨中,NO与O2要发生化学反应生成NO2,所以分子数目不应该由两种气体的初始量来直接加合.
